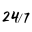轉載從: Tech News 科技新報
冷凍是保存食物、生物組織最簡單方法之一,但冰晶的形成會破壞細胞,這也導致許多物品無法冷凍保存,不過麻省總醫院工程中心(MGH-CEM)開發出一種新方法解決這個問題。在一些測試中,研究團隊成功將水基溶液以低於冰點的溫度保存,卻同時保持液體形態而不會形成冰晶。
凍結對液體來說有好有壞,從好的方面來看,寒冷意味著減緩某些代謝過程和化學反應,這代表細菌不會生長,組織也不會迅速降解,但從另一方面來說,因為凍結導致細胞之間形成冰晶,細胞也會因此損壞。
這便是組織、器官、藥品和一些食物無法冷凍保存的原因。如果能找到方法以低於冰點的溫度保存卻又不會形成冰晶,人們將能更長時間儲存和運輸這些物品,這正是 MGH 研究團隊希望達到的目標。
但該怎麼做才能讓冰晶無法形成?
首先,我們得先來複習一下「結冰」的過程:以常見的水為例,當溫度降至 0°C(32°F)時,水和水基溶液便會開始凍結,過程會從與空氣接觸的表面開始,當表面水分子遇到過冷空氣開始形成冰晶,接著逐漸擴散到鄰近分子,直到水凍結形成冰塊。基於此項概念,MGH 提出一個非常簡單的假設──如果不讓液體表面和空氣接觸呢?
初次測試中,團隊運用碳氫基礎油(hydrocarbon-based oil)密封 1 毫升水樣品表面,結果發現樣品可在 -13°C 儲存長達一週而不會出現冰晶,團隊將這種方法稱為「深度過冷」(deep supercooling)。
共同作者 O. Berk Usta 指出,深度過冷簡單來說,其實只是運用不會和水混合的溶液(像是礦物油)覆蓋液體表面,阻止水和空氣直接接觸,進而阻止冰晶形成的場合,「這種方法出乎意料的簡單、實用和低成本,同時還能實用在許多醫療和食品保存,以及過去一些無法實現的基礎實驗。」
第一次實驗的基礎上,研究人員測試了更複雜的油類和更單純的碳氫化合物(hydrocarbons),像是醇類和烷烴(alkanes),結果團隊成功將 1 毫升水和細胞懸浮樣品過冷至 -20°C 並持續 100 天,即使將液體量提升至 100 毫升時,樣品也成功冷藏長達一週。
團隊接著繼續測試如何保存如紅血球的物質,初步實驗中,他們成功將 100 毫升紅血球懸浮液在 -13°C 下過冷保持 100 天,這大約是現有保存做法能達到最大天數(約 42 天)的兩倍之多,他們現在正打算將樣本的體積增加到 300~500 毫升,以更符合臨床應用的相關需求。
團隊同時也在努力將這種方法應用於其他細胞,或是其他相關大型組織和整個器官,如肝臟。考量到醫學和食品保存的潛在應用,團隊也相信深度過冷可在沒有昂貴和複雜的高壓設備時,用來協助研究低溫下的液態化學反應。
這項研究已發表在《Nature Communications》期刊。
- Supercool technique keeps liquids liquid well below freezing
- Novel approach keeps liquids from freezing at very low temperatures for extended periods
(首圖來源:pixabay)