轉載從: Tech News 科技新報
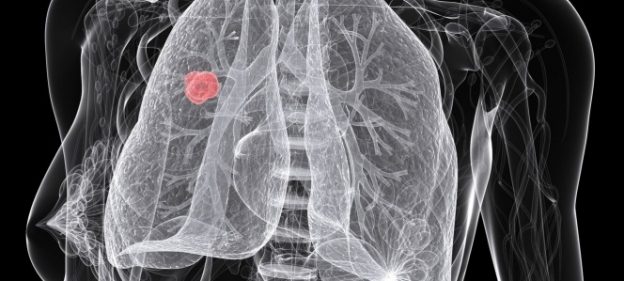
肺癌初期常因無明顯症狀而未能及時發現,導致許多肺癌患者發現時已是中晚期癌症,確診後往往無法存活超過一年。近年來拜分子生物學與基因醫學突飛猛進之賜,新一代「標靶藥物」改寫許多癌症病患的命運,它們能針對致病的突變基因對症下藥,有效提升治療成效、延緩病情惡化並且降低副作用,延長病患壽命、改善生活品質。
台灣每年新增約一萬名肺癌病患,以「肺腺癌」佔多數,肺腺癌中又以「表皮生長因子」(EGFR)基因變異患者佔多數(約一半),可以 EGFR 之標靶藥物治療,此外有約 5% 屬於「間變性淋巴瘤激酶(ALK)基因變異」(ALK 陽性,註 1),則以 ALK 標靶藥物治療。
最早(2013 年)用於治療 ALK 基因變異之肺癌的標靶藥物為美國輝瑞公司(Pfizer)生產的標靶藥物「截剋瘤」(Crizotinib),相較於傳統化療藥物能延緩病情之惡化且副作用較小,使用此藥物能提高病患生活品質。然而服藥約半年後腫瘤通常會產生抗藥性開始惡化。
約於兩年後(2015 年)諾華公司研發出新一代 ALK 標靶新藥 「立克癌」(Ceritinib),藥效更好,用於治療某些已對截剋瘤產生抗藥性的病人也有療效,可以穩定控制病情超過一年之後才產生抗藥性。
最近日本武田製藥公司(Takeda Pharmaceutical Company)旗下的美國癌症藥品製造商 Ariad 公司進一步研發出一款幾乎可以對付所有已知的截剋瘤抗藥性的新藥 Brigatinib,能幫助病患繼續控制對截剋瘤產生抗藥性之腫瘤,甚至對於將近一半已產生「腦部轉移」的病患也有療效。FDA 基於 Brigatinib 於第二期臨床試驗的優異表現(註 2),已於今年 4 月決定加速批准該藥的審核(註 3),使該藥可儘快上市救治病患。但該新藥之持續核准仍有待後續臨床試驗對治療的效益進一步驗證和描述。武田製藥也承諾將在全球持續開發 Brigatinib,以協助更多需要此藥物的患者獲得有效的治療。
註 1:ALK 是一種表現於細胞膜上的「受體酪胺酸激酶」(receptor tyrosine kinase),對發育中的中樞和周邊神經系統之發育扮演重要功能,於成體之正常功能尚不清楚,但在許多癌症皆有異常活化的情形。ALK 最早發現於淋巴瘤中有基因的變異,後來陸續於肺癌、腸癌以及乳癌均有發現。
註 2:一般藥品需進行至第三期臨床試驗,包含上千人的受試者。而本次第二期臨床試驗僅有 222 位受試者。
註 3:美國 FDA 為滿足病患對於醫療的迫切需求,在 1992 年訂定了加速核准(Accelerated approval)制度 ,只要在科學證據的支持下,可允許縮短藥品研發之時程,使藥品提早上市。但獲得加速核准的新藥後續仍必須提出能支持對嚴重、危及生命之疾病有療效與安全性之證據,且確實給予患者優於現行療法之治療。
(首圖來源:Flickr/Oregon State University CC BY 2.0)